М. В. Майоров, Женская консультация городской поликлиники № 5, г. Харьков
«Non quaerit aeger medicum eloquentem, sed sanantem»
(«Больной ищет не красноречивого врача, а способного вылечить», лат.)
После того как Fraenkel в 1903 г. установил значение желтого тела для имплантации яйцеклетки и поддержания беременности, в 1929 г. появилось сообщение о действии экстракта из желтого тела на слизистую матки. В 1934 году были выяснены химическое строение и синтез действующего вещества, названного прогестероном, а в 1935 г. за разработку методики его синтеза A. Butenandt и его группа были удостоены Нобелевской премии. Само название этого гормона второй фазы менструального цикла отражает основную точку его приложения в организме: «pro gestatio» («для беременности»).
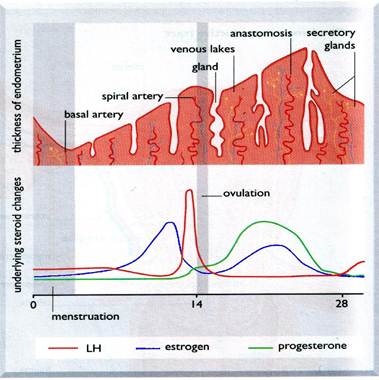
Физиологический эффект прогестерона заключается, в первую очередь, в секреторной трансформации эндометрия. Он тормозит вызванную эстрогенами пролиферацию слизистой, стимулирует секрецию эндометриальными железами богатой гликогеном слизи и путем разрыхления субгландулярной стромы подготавливает слизистую к имплантации бластоциста. Другой важный механизм действия прогестерона обеспечение «покоя» миометрию посредством понижения его чувствительности к окситоцину (так называемый «эффект поддержания беременности»). Вне беременности прогестерон синтезируется в основном желтым телом. За сутки оно секретирует до 25 мг прогестерона. При беременности активность желтого тела на ранней стадии эмбриогенеза поддерживает трофобласт, который продуцирует хорионический гонадотропин человека (ХГЧ). Под действием ХГЧ желтое тело синтезирует и секретирует прогестерон в достаточном, чтобы предотвратить отторжение эндометрия, количестве. В противном случае отторжение произойдет через 1012 суток после овуляции (А. Я. Сенчук, Б. М. Венцковский и др.).
В результате действия прогестерона не сужаются спиральные артерии и не некротизируется эндометрий с последующей менструацией. При нормальных условиях течения беременности трофобласт трансформируется в синцитиотрофобласт, превращающийся в фетоплацентарную систему. В течение первых 810 недель хорион продуцирует большое количество ХГЧ, все сильнее стимулируя желтое тело, повышающее в ответ на это секрецию прогестерона. Продукция прогестерона плацентой начинается с 810 недель и с этого времени течение беременности перестает всецело зависеть от желтого тела. Она не прерывается даже после удаления яичников! Содействие оказывают и надпочечники, кора которых осуществляет дополнительную продукцию прогестерона. Поступая в кровь, прогестерон связывается с альбумином и транспортным белком транскортином, метаболизируется в печени путем связывания с глюкуроновой и серной кислотами (основные метаболиты прегнандиол и прегнанолол), а затем выводится с мочой.
Биологические эффекты прогестерона при беременности весьма многообразны: торможение продукции ФСГ, блокирующее рост новых фолликулов, усиление васкуляризации эндометрия и пролиферации и секреторной деятельности желез эндометрия, в результате чего в секрете возрастает концентрация липидов и гликогена, необходимых для развития эмбриона, ингибирования опосредованной через Т-лимфоциты реакции отторжения тканей, задержка в организме натрия и воды, выраженный пирогенный эффект. В I триместре беременности прогестерон снижает порог возбудимости мышечных волокон, что в совокупности с повышением тонуса гладкомышечных волокон шейки матки способствует вынашиванию беременности. Во II и III триместрах высокий уровень прогестерона тормозит сократительную деятельность матки благодаря β-адренорецепторному ингибирующему эффекту, который приводит к угнетению спонтанной и индуцированной активности миометрия. Прогестерон является предшественником стероидных гормонов плода в период беременности, а также эстрогенов, андрогенов, альдостерона и некоторых других гормонов коры надпочечников. Однако и прогестерон, и его ближайшие аналоги, состоящие из 20 углеродных атомов, не проявляют ни эстрогенной, ни андрогенной активности (для прогестерона, напротив, характерна антиэстрогенная активность).
Еще не так давно гестагены воспринимались только как гормоны, способствующие имплантации оплодотворенной яйцеклетки в эндометрий и вынашиванию беременности, в связи с чем применялись в основном для лечения угрозы прерывания беременности. Изучение процессов синтеза и метаболизма половых стероидных гормонов, экспрессии рецепторов к этим гормонам в различных органах и тканях, особенностей взаимодействия стероидов с этими рецепторами обеспечило раскрытие механизмов развития ряда дисгормональных заболеваний у женщин и создание лекарственных средств, обладающих необходимыми терапевтическими свойствами. Так, дефицит прогестерона зачастую имеет место при бесплодии и невынашивании беременности и, соответственно, именно эти патологические состояния, в первую очередь, являются показанием к применению прогестагенов. Относительный или абсолютный дефицит прогестерона обусловливает развитие гиперпролиферативных процессов эндометрия, поэтому именно гиперпластические процессы, а также состояния с высоким риском их развития являются второй по значимости группой показаний к применению прогестагенов (Т. Ф. Татарчук, Я. П. Сольский, 2003).
В настоящее время сформулированы основные показания к применению прогестагенов в гинекологической практике [16, 17]:
- гиперпластические процессы эндометрия;
- эндометриоз;
- миома матки;
- протекторное воздействие на эндометрий при заместительной гормональной терапии (ЗГТ);
- профилактика «синдрома вспышки» при применении агонистов ГнРГ (по данным литературы, отмечается в 1015% случаев за счет кратковременного повышения уровня эстрогенов на 1012-й день после 1-й инъекции агониста и проявляется в виде межменструальных кровянистых выделений и некоторого усиления болей при эндометриозе);
- альгодисменорея;
- предменструальный синдром;
- некоторые виды дисгормональных заболеваний молочных желез (ДЗМЖ).
В арсенале врача в последнее время имеется достаточно большой выбор препаратов, обладающих прогестагенным действием, но различающихся как химической структурой, так и особенностями биологических эффектов. Это предопределяет необходимость дифференцированного подхода к выбору конкретного препарата при той или иной патологии с учетом индивидуальных особенностей каждой пациентки.
Спектр прогестагенов, применяемых в клинической практике, включает природные и синтетические препараты [17]:
1. Натуральный прогестерон: для парентерального применения (мази, гели, инъекции) и для перорального применения (микронизированный утрожестан)
2. Синтетические прогестагены:
а) сходные по структуре с прогестероном:
- ацетилированные (медроксипрогестерона ацетат, мегестрола ацетат, ципротерона ацетат, хлормадинона ацетат, медрогестон);
- неацетилированные (дидрогестерон дуфастон);
непрегнановые производные (демегестон, промегестон, номегестрола ацетат);
б) сходные по структуре с тестостероном:
- эстрановые производные (норэтиндрон примолют-нор, норэтинодрел, линестенол, норэтиндрона ацетат, этинодиола диацетат)
- гонановые производные (левоноргестрел, дезогестрел, гестоден, норгестимат);
Имеющиеся в достаточном ассортименте синтетические прогестагены, классифицируемые по строению исходной стероидной молекулы, из которой их получают, обладают различной способностью связываться с различными рецепторами и различным спектром гормональных эффектов (табл. 1).
Таблица 1. Спектр гормональных эффектов прогестагенов (Donald P.M cDonnel, 2000; OettelM., SchillingerE., 1999; YenS. S. C. et al., 1999)
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Дифференцированные подходы к применению прогестагенов определяются:
- взаимодействием со специфическими прогестероновыми рецепторами (табл. 2 и 3);
- взаимосвязью с неспецифическими рецепторами андрогенов, эстрогенов, кортизола, альдостерона;
- влиянием на энзимы, участвующие в метаболизме стероидов.
Таблица 2. Степень сродства различных прогестагенов к рецепторам прогестерона в матке (Прилепская В. Н. (ред.) «Гормональная контрацепция», М., 1998)
|
Таблица 3. Минимальная доза прогестагена, оказывающая эффект на эндометрий
|
Достижение максимального эффекта в лечении тех или иных патологических состояний при минимальном нежелательном системном воздействии лекарств на организм всецело зависит от правильного выбора препарата, оптимальной дозы и режима его введения в каждом конкретном случае. Подавление митотической активности эндометрия, необходимое при лечении гиперпластических процессов эндометрия, а также для профилактики его гиперпролиферации при проведении эстроген-заместительной терапии обеспечивается за счет следующих фармакологических свойств прогестагенов: стромальной супрессии эндометрия, снижения активности эстрогенных рецепторов на ядерной мембране, увеличения продукции эстрадиолконвертирующих энзимов, угнетения инкорпорации тимидина клетками эндо- и миометрия и снижения их чувствительности к эстрогенам, угнетения матричных металлопротеиназ-ферментов, обеспечивающих процессы ремоделирования в тканях с физиологическим отторжением в эндометрии. Это особенно важно для предупреждения гетеротопической имплантации эндометрия при лечении и профилактике эндометриоза (Т. Ф. Татарчук и соавт., 2003).
|
Режимы, схемы применения и пути введения различных прогестагенов (табл. 4) определяются биологическими эффектами различных доз препаратов, имеющимися данными о чувствительности к прогестагенам эпителия и стромы эндометрия в различные фазы менструального цикла и, соответственно, той целью, которую ставит перед собой врач, назначая лечение патологического состояния с непременным учетом патогенеза.
Так как гестагены обычно назначаются более-менее длительными курсами, следует обязательно учитывать имеющиеся противопоказания, встречающиеся побочные явления, своевременно обеспечивая их устранение, медикаментозную и алиментарную коррекцию.
Широко применяя гестагены в последние годы, клиницисты встретились с развитием патологического симптомокомплекса, описанного в литературе как синдром непереносимости гестагенов (СНГ). Этот синдром включает психопатологический, метаболический и физикальный компоненты, обусловленные системным действием различных гестагенов или их метаболитов на организм женщины. Поэтому научные исследования, направленные на поиск путей преодоления СНГ, развиваются в двух направлениях: применение новых прогестагенов с максимально селективным прогестероновым действием, а также использование новых путей введения гормонов, в частности, местного, что обеспечивает минимальное системное влияние на организм.
Новое это не всегда «хорошо забытое старое», поэтому с таким интересом были восприняты недавние весьма интересные исследования о роли прогестерона и других гестагенов в формировании адекватного иммунного ответа на ранних стадиях беременности. Именно в присутствии этого гормона активированные лимфоциты вырабатывают специфический белок прогестерон-индуцированный блокирующий фактор (PIBF), который оказывает антиабортивное действие. Общепризнанно: для нормального исхода беременности необходимо, чтобы иммунная система матери была способна ее распознать. При нормально протекающей беременности в лимфоцитах периферической крови присутствуют прогестероновые рецепторы, причем доля клеток, содержащих эти рецепторы, увеличивается по мере увеличения срока гестации. У женщин с высоким риском преждевременного прерывания беременности доля клеток, содержащих прогестероновые рецепторы, существенно ниже, чем у здоровых женщин, имеющих такой же срок беременности. PIBF изменяет баланс цитокининов в иммунной системе, обеспечивая нормальное течение беременности.
Именно в разумном сочетании хорошо известного и нового, «доселе неведомого», состоит один из основных принципов «аrs medica» искусства врачевания.
- Бороян Р. Г. Клиническая фармакология для акушеров-гинекологов. М.: Мед. информ. агентство, 1999.
- Деримедведь Л. В., Перцев И. М., Шуванова Е. В., Зупанец И. А., Хоменко В. Н. Взаимодействие лекарств и эффективность фармакотерапии. Харьков: Мегаполис, 2002.
- Коханевич Е. В. (ред.) Актуальные вопросы гинекологии. К.: Книга-плюс, 1998.
- Майоров М. В. Современные методы торможения лактации // Медицина и…. 1999. № 1 (4). С. 3537.
- Майоров М. В. Эндометриоз: современные представления о патогенезе, диагностике и лечении // Медицина и…. 2000. № 1 (6). С. 914.
- Майоров М. В. Альгодисменорея: патогенез, диагностика и лечение // Провизор. 2000. № 16. С. 2627.
- Майоров М. В. Предменструальный синдром: загадки патогенеза, проблемы терапии // Провизор. 2001 № 13. С. 3839.
- Майоров М. В. Некоторые аспекты гормональной контрацепции // Провизор. 2002 № 1 С. 4344.
- Майоров М. В. Миома матки: хирургический экстремизм или медикаментозный консерватизм? // Провизор. 2002. № 7. С. 3638.
- Майоров М. В. Синдром поликистозных яичников: современный взгляд // Провизор. 2002. № 16. С. 3941.
- Майоров М. В. Неконтрацептивные свойства оральных контрацептивов // Провизор. 2003. № 11. С. 1618.
- Майоров М. В. Заместительная гормональная терапия: панацея или очередная дань моде? // Провизор. 2003. № 20. С. 4246.
- Манухин И. Б., Тумилович Л. Г., Геворкян М. А. Клинические лекции по гинекологической эндокринологии. М.: Мед. информ. агентство, 2001.
- Савицкий Г. А., Савицкий А. Г. Миома матки. Проблемы патогенеза и патогенетической терапии. Санкт-Петербург, 2000.
- Серов В. Н., Прилепская В. Н. и др. Гинекологическая эндокринология. Москва, 1998.
- Татарчук Татьяна. Принципы применения прогестагенов в гинекологии // Доктор. 2001. № 3(7). С. 3942.
- Татарчук Т. Ф., Сольский Я. П. Эндокринная гинекология (клинические очерки), часть 1. Киев, 2003.
- Шамбах Х., Кнаппе Г., Карол В. (ред.) Гормонотерапия / Пер. с нем. М.: Медицина, 1988.
- Donald P. McDonnel. Molecular pharmacology of estrogen and progesterone receptors // Menopause Biology and Pathobiology. San Diego-Tokyo: Academic press, 2000. P. 311.
- Yen SSC., Jaffe R. B., Barbieri R. L.R eproductive Endocrinology. Philadelphia-Tokyo: W. B. Saunders Company, 1999.