Комплексное исследование, позволяющее определить уровень стероидных гомонов (андрогенов и эстрогенов) в суточной моче, а также клинически значимых метаболитов андрогенов и их расчетные соотношения. У женщин эстрогены обеспечивают нормальное развитие и функционирование репродуктивной системы, у мужчин участвуют в регуляции функций простаты и яичек. Андрогены отвечают за развитие мужских вторичных половых признаков и вирилизацию при их избытке у женщин либо при нарушении их превращения в эстрогены.
Исследование не предназначено для пациентов в возрасте до 16 лет. При регистрации заявок для исследования стероидных гормонов у женщин обязательно указывать наличие/отсутствие беременности.
Андрогены и их метаболиты:
- дегидроэпиандростерон (ДГЭА),
- андростендион,
- тестостерон,
- андростерон,
- эпиандростерон,
- этиохоланолон,
- андростерон/этиохоланолон,
- тестостерон/эпитестостерон.
Газовая хроматография-масс-спектрометрия (ГХ-МС).
Мкг/сут. (микрограмм в сутки), мг/сут. (миллиграмм в сутки).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- При отсутствии указаний врача женщинам рекомендуется проводить исследование на 3-5 день менструального цикла.
Общая информация об исследовании
Андрогены и их метаболиты
Андрогены – стероидные половые гормоны, производимые половыми железами: яичками у мужчин и яичниками у женщин. У обоих полов синтез андрогенов может происходить в клетках сетчатого слоя коры надпочечников. Отвечают за развитие мужских вторичных половых признаков и вирилизацию при их избытке у женщин либо при нарушении их превращения в эстрогены.
Дегидроэпиандростерон (ДГЭА) образуется в надпочечниках. Малая часть (5-6 %) имеет гонадное происхождение. ДГЭА – продукт гидроксилирования 17-гидроксипрегненолона. ДГЭА — прогормон в синтезе половых стероидов: андрогенов (андростендиона и тестостерона) и эстрогенов (эстрадиола и эстрона). Проявляет слабые андрогенные свойства (в 15 раз слабее тестостерона). Повышение уровня его экскреции служит важным показателем гиперандрогении надпочечникового генеза. Большая часть гормона конвертируется в дегидроэпиандростерон-сульфат.
Тестостерон – главный андрогенный стероидный гормон. Около 57 % тестостерона, поступающего в кровь, связывается с глобулином, связывающим половые стероиды (ГСПС). Эта связь мешает проникновению гормона в андроген-чувствительные клетки, что практически блокирует его андрогенную активность. Остальная часть тестостерона биологически доступна: связанный с альбумином тестостерон (около 40 %); свободный тестостерон (примерно 3 %). В тканях тестостерон превращается в активную форму 5-альфа-дигидротестостерон.
Эпитестостерон – изомер тестостерона со слабой андрогенной активностью, отражающий метаболизм преимущественно эндогенного тестостерона. Применяется для расчета соотношения тестостерон/эпитестостерон.
Андростерон – метаболит андростендиона и/или тестостерона, образующийся в ходе 5α-резуктазной реакции. Обладает низким андрогенным действием (в 5-7 раз слабее тестостерона), стимулирует развитие вторичных мужских половых признаков. Определение андростерона применяют для оценки уровня продукции андрогенов в организме и расчета соотношения андростерон/этиохоланолон.
Эпиандростерон (изоандростерон) – изомер андростерона и метаболит ДГЭА со слабой андрогенной активностью (в 5-6 раз меньше, чем у андростерона), отражающий активность 5 альфа-редуктазы.
Этиохоланолон – метаболит андростендиона, образующийся в ходе 5β-редуктазной реакции. Не обладает андрогенной активностью. Определение уровня этиохоланолона применяют для оценки функции надпочечников и расчета соотношения андростерон/этиохоланолон.
Соотношение андростерон/этиохоланолон отражает соотношение активности ферментов 5α-редуктазы и 5β-редуктазы, которые превращают тестостерон или андростендион в активные и неактивные формы соответственно. Применяют для оценки эффективности вирилизующей трансформации тестостерона, андростендиона и ДГЭА.
Соотношение тестостерон/эпитестостерон отражает емкость ферментных систем, способных трансформировать тестостерон в неактивные метаболиты. Применяется для оценки эффективности метаболизма тестостерона и в особенности при применении экзогенных форм гормона.
Эстрогены – стероидные половые гормоны, преобладающие в женском организме. Синтез эстрогенов у женщин осуществляется фолликулярным аппаратом яичников, а у мужчин в основном яичками (до 20 %). У женщин эстрогены обеспечивают нормальное развитие и функционирование репродуктивной системы, а у мужчин участвуют в регуляции функций простаты и яичек. Эстрогены представлены тремя формами: эстроном (фолликулин) — Е1, эстрадиолом — Е2 и эстриолом — Е3, имеющими разную физиологическую активность: Е2 ˃ Е3 ˃ Е1.
Прогестагены – стероидные половые гормоны, производимые у женщин желтым телом яичников, плацентой и частично корой надпочечников. Прогестагены у женщин обеспечивают возможность наступления и поддержания беременности, регулируя переход слизистой оболочки матки из фазы пролиферации в секреторную фазу и способствуя образованию нормального секреторного эндометрия у женщин. Обладают антиэстрогенными, антианрогенными и антигонадотропными свойствами. У мужчин прогестерон вырабатывается в небольших количествах корой надпочечников и яичками как промежуточный продукт синтеза тестостерона и кортизола, самостоятельно принимает участие в работе центральной нервной системы.
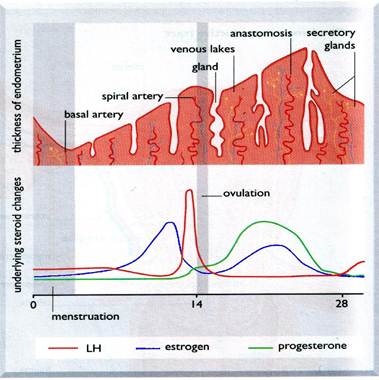
Основным гормоном гранулезы является эстрадиол, образуемый из предшественника тестостерона. В меньшем количестве гранулеза образует эстрон, из которого в печени и плаценте образуется эстриол. Клетки гранулезы образуют в малых количествах и прогестерон, необходимый для овуляции, но главным источником прогестерона являются клетки желтого тела, регулируемые гипофизарным лютропином. Секреторная активность этих эндокринных клеток характеризуется выраженной цикличностью, связанной с женским половым циклом.
Эстрогены необходимы для процессов половой дифференцировки в эмбриогенезе, полового созревания и развития женских половых признаков, установления женского полового цикла, роста мышцы и железистого эпителия матки, развития молочных желез. Они регулируют половое поведение, овогенез, процессы оплодотворения и имплантации яйцеклетки, развитие и дифференцировку плода, нормальные роды.
Благодаря геномному механизму действия, эстрогены подавляют резорбцию кости, оказывают общее анаболическое действие, хотя и более слабое, чем андрогены. Негеномый механизм действия эстрогенов ведет к задержке в организме азота воды и солей. Одним из важных негеномных эффектов эстрогенов является активация под их влиянием NO-синтетазы и образование оксида азота в коронарных сосудах, что обеспечивает профилактику развития у женщин ишемической болезни сердца.
Эстрогены модулируют секрецию инсулина и внутриклеточный гомеостазис кальция. Распространенность рецепторов эстрогенов на мембранах разных типов клеток организма (костные, мышечные, секреторные, нервные, соединительной ткани и крови) и, соответственно, множественность эффектов гормонов в организме объясняют причины многочисленных функциональных изменений, происходящих в женском организме при климаксе, когда секреция эстрогенов резко снижается.
Прогестерон является гормоном сохранения беременности (гестагеном), так как ослабляет готовность мускулатуры матки к сокращению. Малые концентрации гормона необходимы и для овуляции. Большие количества прогестерона, образующиеся желтым телом, подавляют секрецию гипофизарных гонадотропинов. Прогестерон обладает выраженным антиальдостероновым эффектом и стимулирует натриурез.
Наиболее характерной особенностью биологического действия прогестерона является его термогенный эффект, проявляющийся в повышении температуры тела на 0,5-0,7 °C при увеличении уровня прогестерона. Основным звеном в процессе инактивации прогестерона является печень, что частично обусловливается чрезвычайно быстрым образованием конъюгированных соединений. Претерпевая частичную инактивацию, прогестерон выделяется в виде биологически неактивных продуктов, главным из которых является прегнандиол. Быстрое исчезновение прогестерона из крови и отсутствие параллельных изменений концентрации его в крови и прегнандиола в моче после внутримышечного введения массивных доз гестерона объясняют в основном продолжительным сохранением его в жировой клетчатке. Выделение указанного стероида в значительных количествах даже после прекращения его продукции в организме подтверждает, что источником его является прегнандиол, аккумулировавшийся в жировой ткани. В настоящее время принята следующая рабочая схема метаболизма прогестерона в печени человека: прогестерон – прегнандион – прегненолон – прегнандиол.
Нарушение синтеза эстрогенов может привести к дисфункции яичников, нарушениям менструального цикла, преждевременному или замедленному половому развитию у женщин; дисфункции придатка и яичек, нарушению сперматогенеза, снижению фертильности и гинекомастии у мужчин; остеопорозу, ожирению, жировой дистрофии печени и бесплодию у обоих полов.
Для чего используется исследование?
- Для выявления уровня гормонов и контроля за ним, диагностики связанных с этим нарушений.
Когда назначается исследование?
- Выявление врождённой и приобретенной дисфункции коры надпочечников;
- лабораторная диагностика надпочечниковой гиперандрогении;
- гипогонадизм, задержка или ускорение полового развития;
- привычное невынашивание, бесплодие у женщин;
- синдром поликистозных яичников;
- гормонпродуцирующие опухоли коры надпочечников, дисфункция придатка и яичек;
- нарушение сперматогенеза;
- снижение фертильности и гинекомастия;
- остеопороз;
- ожирение, жировая дистрофия печени;
- бесплодие.